O que todo profissional da saúde precisa saber em diagnóstico genético em todas fases da vida do paciente

- Em qualquer momento da vida pode ser necessário um diagnóstico genético.
- É possível prevenir que uma doença hereditária seja transmitida aos filhos através do planejamento familiar, obter o diagnóstico preciso de doenças genéticas e câncer.
Baixe nosso ebook

As doenças genéticas afetam entre 6-8% da população. Estima-se que 40% dos pacientes recebem um diagnóstico errado ao menos uma vez, complicando seus quadros clínicos. Muitos padecem por não receber um diagnóstico a tempo.
De forma contínua a medicina ganha precisão para o diagnóstico e tratamentos de doenças genéticas. No entanto, esse conhecimento ainda não chegou a uma parcela grande dos profissionais da saúde. Mudar esse cenário permitirá reduzir as complicações do diagnóstico tardio e, inclusive, prevenir doenças sem cura.
A partir de um diagnóstico preciso, é possível determinar melhor o prognóstico clínico e proporcionar um tratamento adequado. Um diagnóstico conclusivo permite ter conhecimento sobre o impacto da doença detectada na vida da pessoa afetada, o risco de acometimento de outros membros da família e opções para o planejamento das futuras gerações.
O diagnóstico também pode reduzir custos para o Sistema de Saúde, pois milhões são gastos em internações, consultas e tratamentos ineficazes devido ao desconhecimento sobre a causa dos sinais e sintomas que os pacientes apresentam, tendo como consequência a impossibilidade de oferecer o tratamento mais efetivo.
Quando é preciso realizar um diagnóstico genético?
Poderíamos dizer que o diagnóstico é preciso na presença de sintomas, porém em algumas fases da vida, como no nascimento, estar um passo à frente pode mudar totalmente a vida do bebê que acaba de chegar ao mundo. Outro momento importante de atuar com o diagnóstico antes mesmo dos sintomas é no planejamento familiar.
Sem dúvida o mais importante é que as famílias conheçam as possibilidades de prevenção para que possam tomar decisões informadas, pois seria um equivoco para os profissionais da saúde tomar essa decisão no lugar do paciente assumindo o que é melhor ou o que cada pessoa deve ou tem condições de fazer.
É possível contar com testes que auxiliam no diagnóstico de doenças genéticas em todas as fases da vida.
Por onde começam os estudos genéticos se queremos prevenir doenças hereditárias?
Na maioria das vezes os estudos genéticos acontecem nas fases pré-natal e neonatal com o objetivo de identificar as doenças de forma precoce, ou seja, antes da manifestação de sintomas através da triagem pré-natal e teste do pezinho, realizado em todos os recém-nascidos.
40% das hospitalizações pediátricas e mortalidade infantil em países desenvolvidos se devem a doenças genéticas. Parker, Samantha E et al.
No entanto, quando se fala em prevenção de doenças genéticas hereditárias, devemos considerar que antes mesmo da gravidez é possível realizar diagnósticos que previnem a passagem de doenças hereditárias presentes na família às futuras gerações. Dessa forma, estamos um passo à frente da manifestação de uma doença no futuro de um recém-nascido.
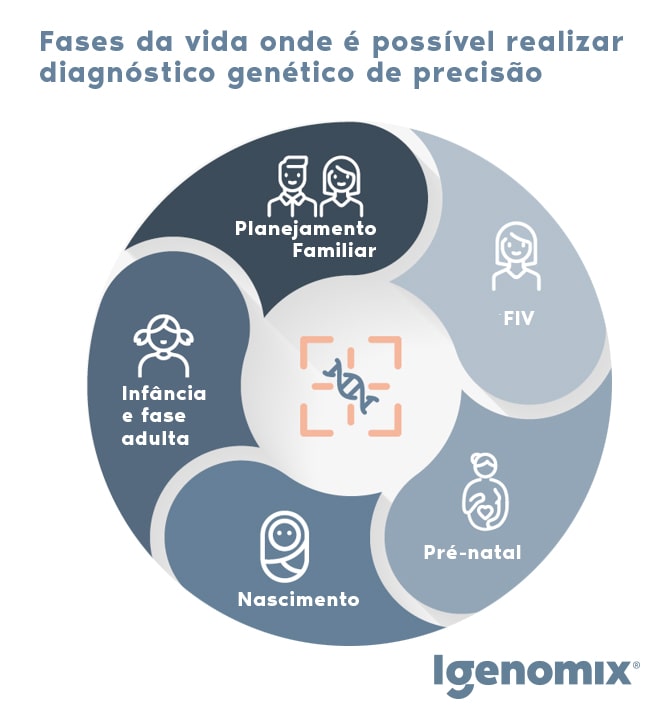
Como é possível detectar o risco de ter filhos com uma doença genética?
Um casal que está planejando engravidar normalmente realiza um check up geral da saúde, porém raramente tem conhecimento que a medicina moderna dispõe de ferramentas para que esse planejamento inclua uma avaliação de risco genético reprodutivo do casal.
88% das crianças nascidas com doenças genéticas não possuem histórico de casos anteriores na família. Martin, Julio et al.
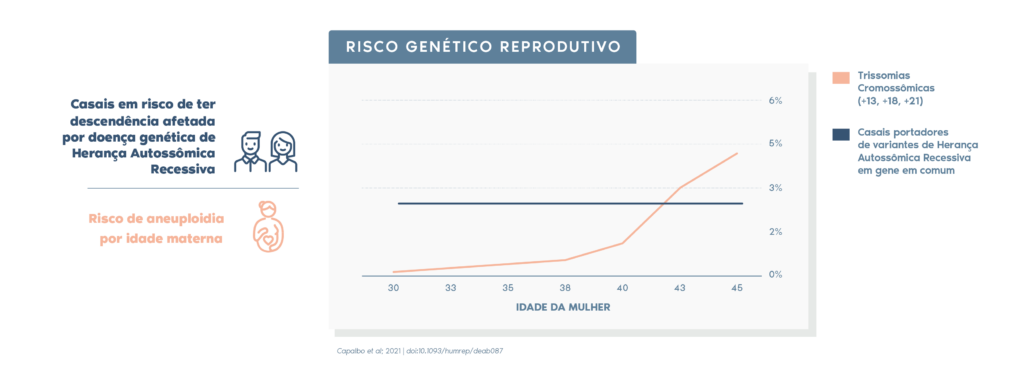
Estima-se que 2,6% dos casais coincidem em variantes patogênicas de herança autossômica recessiva no mesmo gene. Ser portador de uma variante patogênica não irá provocar a doença na pessoa, no entanto se um bebê receber essa variante dos dois progenitores portadores, a criança seria afetada pela doença que pode nunca ter sido manifestada na família.
Alguns podem considerar esse risco populacional baixo, outros vão preferir tirar essa dúvida realizando o teste de compatibilidade genética do casal, já que ao identificar o risco é possível prevenir a passagem da doença aos filhos. Por isso é importante que as famílias sejam informadas.
Se por um lado, para a população geral pode existir uma discussão sobre a relevância de uma avaliação do risco, existe uma parcela importante da população que sempre deve ser orientada, sem exceção. É o caso de casais consanguíneos ou com casos de doenças genéticas até terceira geração, pois nessas situações o risco de hereditariedade de doenças pode ser elevado.
Nem sempre um casal é totalmente consciente de um potencial risco reprodutivo aumentado. Por essa razão, o aconselhamento genético antes de iniciar as tentativas de gravidez de um casal é um recurso importante para tomar a decisão de realizar qualquer teste genético. Dessa forma existirá uma orientação individualizada sobre os prós e contras de um painel de portadores, também conhecido como teste de compatibilidade genética.
Diante de um resultado de painel de portadores que aponte uma elevação de risco de doenças genéticas nos filhos, assim como em famílias com o diagnóstico de uma doença genética que afeta um único gene, na maioria das vezes é possível evitar hereditariedade através da análise genética do embrião na fase pré-implantacional, que ocorre após a fecundação do óvulo e antes da transferência do embrião ao útero materno. O que nos leva para a próxima fase de diagnóstico no ciclo da vida.
Risco de aborto e infertilidade
A linha laranja do gráfico acima, referente ao risco de alterações cromossômicas, aumenta com a idade materna. Este mesmo tipo de alterações, que são denominadas aneuploidias, são a principal causa de perdas gestacionais durante o primeiro trimestre de gravidez.
Mulheres que pretendem adiar o momento de ter filhos precisam ser orientadas sobre a diminuição gradual da qualidade dos seus óvulos e o consequente impacto no aumento de risco de aborto e infertilidade.
Atualmente, a opção de congelamento de óvulos tem sido amplamente difundida como uma forma de aumentar a probabilidade de uma gravidez tardia com óvulos próprios.
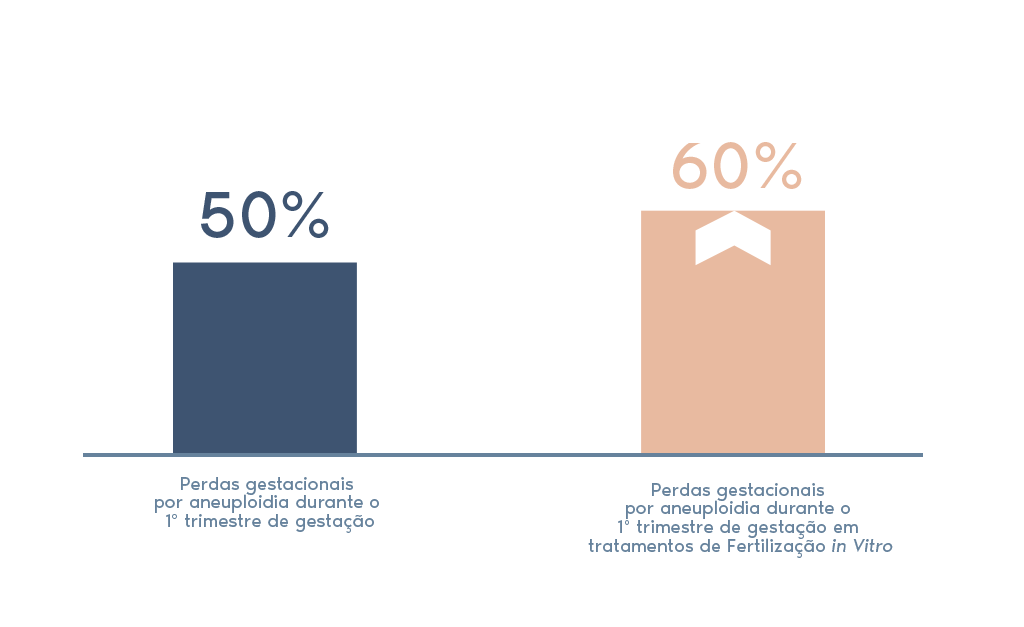
Em caso de uma perda gestacional, especialmente em caso de repetição, analisar o produto do aborto é importante para identificar uma possível origem cromossômica e ajudar o clínico a estabelecer um manejo adequado.
Atualmente existem duas formas de realizar a análise cromossômica do material de aborto:
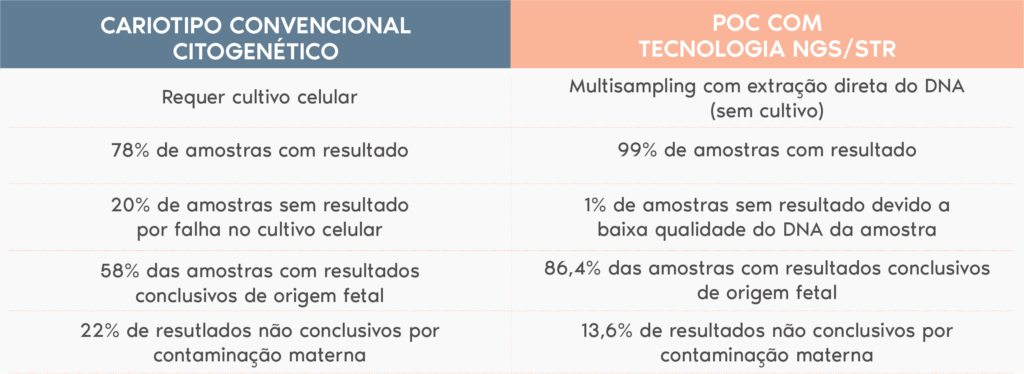
Como é possível detectar uma doença antes mesmo da gravidez ter acontecido?
A prevenção de doenças genéticas é um avanço da ciência que existe há mais de 10 anos, no entanto grande parte dos profissionais da saúde ainda desconhecem essa possibilidade que pode salvar vidas e mudar a história das próximas gerações.
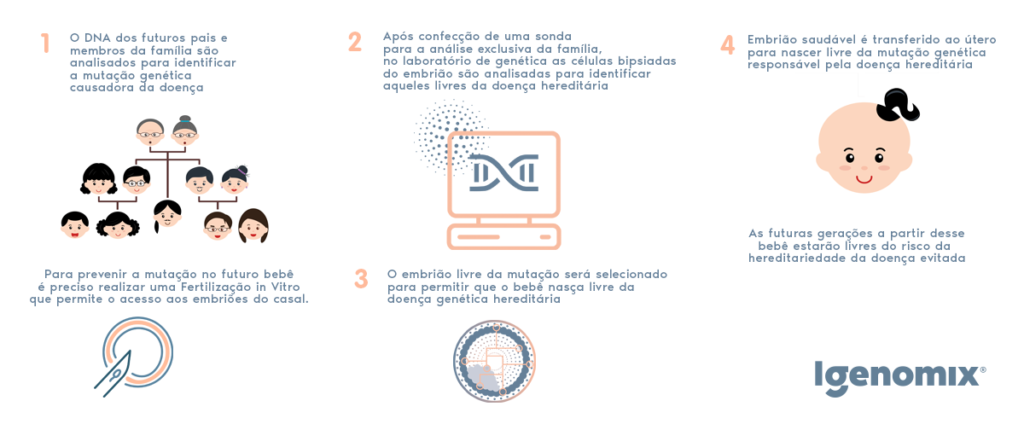
Através de tratamentos Fertilização in Vitro (FIV) é possível prevenir síndromes cromossômicas, abortos e falhas de implantação a partir da análise de algumas células dos embriões com o teste PGT-A.
Já o procedimento de prevenção de doenças gênicas é realizado por meio da análise embrionária para doenças monogênicas (PGT-M). Para tanto é necessário ter um diagnóstico genético do distúrbio que se pretende prevenir nos filhos e a constatação da hereditariedade da doença diagnosticada.
Qual o benefício de uma triagem genética durante a gestação?
Os testes de triagem pré-natal, assim como os testes genéticos em geral, estão cada dia mais acessíveis para a população. A detecção de condições genéticas durante a gestação permite que medidas sejam tomadas para que a criança que irá nascer tenha os recursos que precisa para um melhor prognóstico, além de preparar os pais para acolher esse futuro bebê e aprender previamente sobre os estímulos e cuidados que serão necessários para seu melhor desenvolvimento e qualidade de vida.
Desde 2016, o Colégio Americano de Genética e Genômica Médica (ACMG) comunicou sua posição em relação ao Teste de Pré-natal Não Invasivo (NIPT), coincidindo com ACOG, SMFM, ISPD e ASHG sobre a importância de informar a TODAS as gestantes que o NIPT é a opção mais precisa para rastrear de forma precoce trissomias nos cromossomos 21, 18 e 13.
ACOG: Colégio Americano de Obstetras e Ginecologistas; SMFM: Sociedade de Medicina Materno-Fetal; ISPD: Sociedade Internacional de Diagnóstico Pré-natal; ASHG: Sociedade Americana de Genética Humana
O tratamento iniciado de forma precoce sempre permitirá um melhor prognóstico e, em ocasiões que dependerão do distúrbio em questão, pode inclusive proporcionar uma qualidade de vida plena.
Qual é o melhor exame para cada situação?

Existe uma ordem específica de escalonamento para a solicitação de testes genéticos, sendo a triagem genética pré-natal o ponto de partida da população geral para o rastreamento de um risco aumentado que proporcionará ao médico as informações para os eventuais próximos passos, quando necessário.
O teste genético de triagem pré-natal é conhecido como NIPT (teste pré-natal não invasivo) e pode ser realizado a partir da décima semana de gestação com o objetivo de descartar o risco de síndromes cromossômicas. No caso do NIPT oferecido pelo laboratório Igenomix, a taxa de confiança para a detecção da Síndrome de Down é de 99,9%.
O início da vida é a fase em que o diagnóstico toma maior importância, pois a maioria das doenças genéticas se manifestam na infância. Por esta razão a triagem neonatal através do teste do pezinho oferecida pelo SUS é obrigatória.
70% das doenças genéticas se manifestam na infância. Nguengang Wakap, Stéphanie et al.
Cerca de 4,5%-6% dos recém-nascidos são afetados por um distúrbio genético. Em muitos casos, se a condição é rastreada precocemente poderiam ser evitadas sequelas irreversíveis para esta criança que apenas começa sua vida.
A Triagem Neonatal tem como objetivo rastrear algumas das enfermidades mais frequentes. O teste que une um rastreamento genético e bioquímico é realizado normalmente entre o 3º e o 5º dia de vida do bebê, sendo o período neonatal considerado até o 28º dia de vida.
A recente notícia da aprovação da ampliação do “teste do pezinho” no Brasil é um marco para o acesso público à análise de uma quantidade maior de doenças (50), porém a implementação total dessa lei aprovada em 2021 ainda levará um tempo para ser oferecida de forma completa na prática. Com a nova lei, o exame passará a abranger 14 grupos de doenças. Essa ampliação ocorrerá de forma escalonada em 5 fases, sendo que o prazo estabelecido pelo Ministério da Saúde para cada fase do processo é de 1 ano.
Mais opções de triagem neonatal estão disponíveis de forma privada e merecem ser informadas às famílias, pois uma triagem mais ampla de doenças permite:
- Diminuir a morbidade e a mortalidade de doenças que podem ser tratadas por meio da realização de uma intervenção precoce para melhorar os desfechos neonatais e de saúde a longo prazo.
- Fornecer um serviço de saúde universal de triagem aos recém-nascidos.
- Identificar recém-nascidos positivos para distúrbios genéticos graves.
- Proporcionar orientação às famílias.
- Realizar o encaminhamento para centros de tratamento.
Por exemplo, o teste genético neonatal oferecido pela Igenomix inclui 104 genes usando tecnologia de Sequenciamento de Nova Geração (NGS) complementa o teste do pezinho para permitir uma abordagem direta de distúrbios genéticos com um diagnóstico preciso para condições que causam sérios problemas de saúde a partir da primeira infância e que são acionáveis, ou seja, que a partir de sua detecção é possível tomar medidas que fazem diferença para o prognóstico e qualidade de vida da criança.
O início da vida é a fase em que o diagnóstico toma maior importância, pois a maioria das doenças genéticas se manifestam na infância. Por esta razão a triagem neonatal através do teste do pezinho oferecida pelo SUS é obrigatória.
70% das doenças genéticas se manifestam na infância. Nguengang Wakap, Stéphanie et al.
Cerca de 4,5%-6% dos recém-nascidos são afetados por um distúrbio genético. Em muitos casos, se a condição é rastreada precocemente poderiam ser evitadas sequelas irreversíveis para esta criança que apenas começa sua vida.
A Triagem Neonatal tem como objetivo rastrear algumas das enfermidades mais frequentes. O teste que une um rastreamento genético e bioquímico é realizado normalmente entre o 3º e o 5º dia de vida do bebê, sendo o período neonatal considerado até o 28º dia de vida.
A recente notícia da aprovação da ampliação do “teste do pezinho” no Brasil é um marco para o acesso público à análise de uma quantidade maior de doenças (50), porém a implementação total dessa lei aprovada em 2021 ainda levará um tempo para ser oferecida de forma completa na prática. Com a nova lei, o exame passará a abranger 14 grupos de doenças. Essa ampliação ocorrerá de forma escalonada em 5 fases, sendo que o prazo estabelecido pelo Ministério da Saúde para cada fase do processo é de 1 ano.
Mais opções de triagem neonatal estão disponíveis de forma privada e merecem ser informadas às famílias, pois uma triagem mais ampla de doenças permite:
- Diminuir a morbidade e a mortalidade de doenças que podem ser tratadas por meio da realização de uma intervenção precoce para melhorar os desfechos neonatais e de saúde a longo prazo.
- Fornecer um serviço de saúde universal de triagem aos recém-nascidos.
- Identificar recém-nascidos positivos para distúrbios genéticos graves.
- Proporcionar orientação às famílias.
- Realizar o encaminhamento para centros de tratamento.
Por exemplo, o teste genético neonatal oferecido pela Igenomix inclui 104 genes usando tecnologia de Sequenciamento de Nova Geração (NGS) complementa o teste do pezinho para permitir uma abordagem direta de distúrbios genéticos com um diagnóstico preciso para condições que causam sérios problemas de saúde a partir da primeira infância e que são acionáveis, ou seja, que a partir de sua detecção é possível tomar medidas que fazem diferença para o prognóstico e qualidade de vida da criança.
Nunca é tarde para obter respostas
As doenças genéticas podem se manifestar na infância e fase adulta. Esses são casos em que é preciso agir de forma rápida e precisa e onde todas as especialidades médicas podem contribuir.
Estima-se que o tempo de diagnóstico de uma doença rara é de 5-7 anos, mas no Brasil a espera chega a 10 anos.
Sintomas pouco específicos para um direcionamento clínico são o maior desafio para realizar um diagnóstico de doença genética. Especialmente quando esses sintomas não se limitam a uma única especialidade médica.
Por isso, quando chegam pacientes ao seu consultório com um histórico de anos em busca de uma resposta, acolha essa pessoa para acompanhá-la em um processo investigativo que englobe uma equipe multidisciplinar, especialmente um geneticista, que pode ser o assessor científico do médico para identificar as tecnologias de diagnóstico mais adequadas para cada caso específico e que pode proporcionar apoio para o aconselhamento genético ao paciente antes e após a realização de eventuais exames genéticos que sejam necessários.
72% das doenças raras são de origem genética. Nguengang Wakap, Stéphanie et al.
O exame de diagnóstico genético para casos difíceis nem sempre será o Sequenciamento Completo do Exoma. Existem painéis de diagnóstico genéticos específicos, como por exemplo, painéis de diagnóstico de precisão para doenças cardiovasculares, endocrinológicas, dermatológicas, assim como para todas as especialidades médicas que permitem ser mais preciso e econômico na investigação de cada caso. Na Igenomix é possível inclusive a personalização de painéis de diagnóstico dependendo da suspeita clínica.
Em escala de abrangência, os exames de diagnóstico disponíveis atualmente são:
- Cariótipo de Banda G: analisa aneuploidias, como a Síndrome de Klinefelter e Síndrome de Down, rearranjos equilibrados como translocações e inversões, além dos rearranjos desequilibrados como deleções e duplicações dentro das limitações do teste.
- Microarray Cromossômico (CMA): aneuploidias, microarranjos cromossômicos, sendo o padrão ouro para a detecção de deleções e duplicações não detectadas no cariótipo ao longo de todo o genoma.
- Análise de gene único: indicado para os casos em que o diagnóstico clínico sugere uma doença monogênica conhecida, como por exemplo a Fibrose Cística.
- Painel de precisão: diagnóstico com tecnologia NGS para a análise de múltiplos genes associados a uma doença, condição ou fenótipo, como por exemplo para o diagnóstico da Carcot-Marie-Tooth.
- Sequenciamento Completo do Exoma: analisa toda região codificadora do genoma, que é a região onde estão a maioria das doenças genéticas conhecidas. Esse exame é indicado quando os sinais e sintomas são muito amplos para a realização de um exame direcionado.
- Sequenciamento do Genoma: o último exame na escala do diagnóstico genético que será solicitado quando o Sequenciamento Completo do Exoma não aportou respostas.
Câncer de origem hereditária
Dentro das doenças genéticas que se manifestam na fase adulta, o câncer de origem hereditária se destaca. Apesar de apenas 10% dos cânceres estarem ligados a mutações genéticas hereditárias, é importante investigar essa possível origem, pois o tratamento do paciente acometido e a história de toda família pode ter um melhor desfecho a partir dessa informação.
Parker, Samantha E et al. “Updated National Birth Prevalence estimates for selected birth defects in the United States, 2004-2006.” Birth defects research. Part A, Clinical and molecular teratology vol. 88,12 (2010): 1008-16. doi:10.1002/bdra.20735
Martin, Julio et al. “Comprehensive carrier genetic test using next-generation deoxyribonucleic acid sequencing in infertile couples wishing to conceive through assisted reproductive technology.” Fertility and sterility vol. 104,5 (2015): 1286-93. doi:10.1016/j.fertnstert.2015.07.1166
Nguengang Wakap, Stéphanie et al. “Estimating cumulative point prevalence of rare diseases: analysis of the Orphanet database.” European journal of human genetics : EJHG vol. 28,2 (2020): 165-173. doi:10.1038/s41431-019-0508-0
Capalbo, A et al. “Clinical validity and utility of preconception expanded carrier screening for the management of reproductive genetic risk in IVF and general population.” Human reproduction (Oxford, England) vol. 36,7 (2021): 2050-2061. doi:10.1093/humrep/deab087


