São diferentes as razões que levam as pessoas a acudirem a um banco de óvulos ou sêmen para realizar o sonho de ter filhos. Independente da razão e dos critérios das características físicas que se avalia para identificar os doadores, é prioritário para as famílias que o óvulo ou espermatozoide doados tenham a maior chance possível de gerar um bebê saudável.
Cerca de 3% dos casais¹ estão em risco de ter uma descendência afetada por doenças hereditárias. Uma cifra que é desconhecida para a maioria da população, que em 80% dos casos, quando têm um filho com uma doença genética, desconheciam ser portadores da mutação que provocou a condição ao seu descendente.
O risco de doenças hereditárias pode ser diminuído através dos tratamentos de reprodução assistida e, quando se trata de selecionar um doador de gametas, esta precaução é fundamental. Aqui apresento detalhes sobre a seleção de doadores e painéis de portadores para banco de óvulos e sêmen.
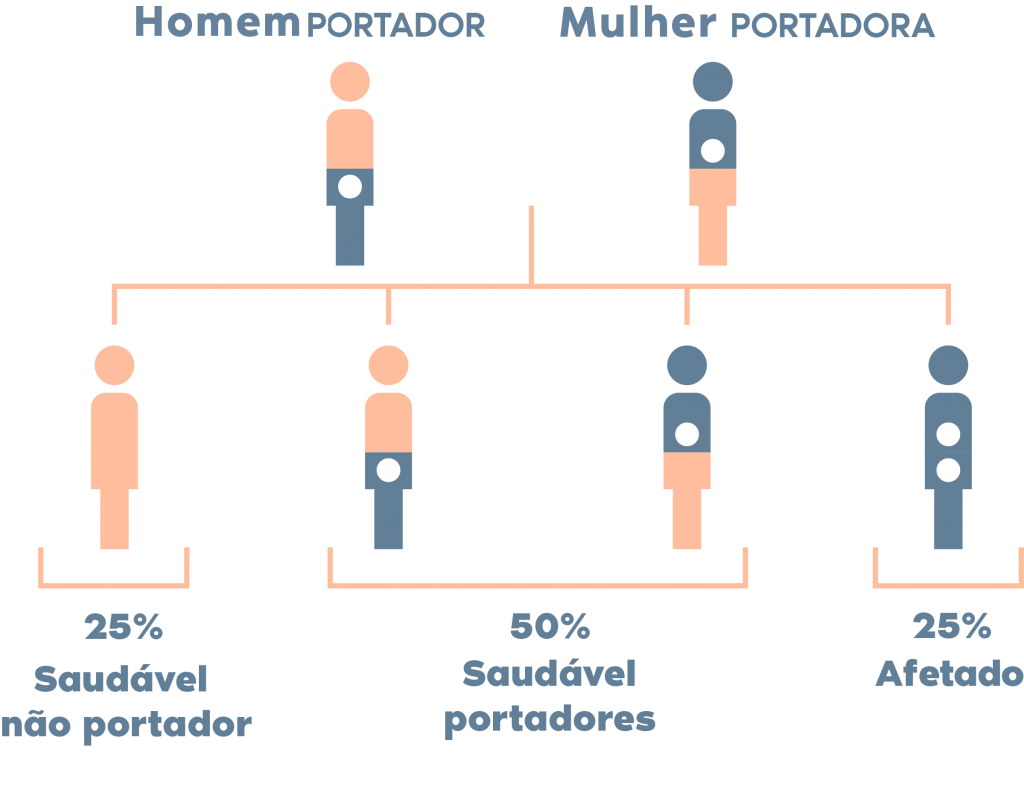 Na formação de um embrião, se o óvulo e o espermatozoide portarem uma mesma mutação recessiva, existe um risco de 25% de nascimento de um bebê afetado por uma doença genética sem cura.
Na formação de um embrião, se o óvulo e o espermatozoide portarem uma mesma mutação recessiva, existe um risco de 25% de nascimento de um bebê afetado por uma doença genética sem cura.

O que deve incluir um protocolo de seleção de doadores de gametas?
Além de uma preocupação em relação às características físicas dos doadores serem similar com a família receptora, os aspectos de saúde para a seleção para um banco de óvulos, também aplicáveis a um banco de sêmen, são:- Doenças hereditárias recessivas e ligadas ao cromossomo X, prevalentes e graves. Sendo fundamental as doenças ligadas ao cromossomo X nos bancos de óvulos, pois as mulheres costumam ser as portadoras assintomáticas de mutações que afetam principalmente o sexo masculino.
- Doenças crônicas, severas ou progressivas que afetam o sistema sensorial, motor ou intelectual e que tenha um fenótipo claramente definido.
- Variantes de significado biológico claro descritas como patogênicas ou provavelmente patogênicas.
- Variantes de distribuição universal, independentemente da origem geográfica do doador.
O que deve excluir um potencial doador ou doadora do programa de doação de gametas?
- Variantes de doenças que existem poucos casos publicados com pouca informação sobre sobrevivência.
- Genes que se associem com um espectro de manifestações clínicas, especialmente se existem correlações fenótipo/genótipo de diferentes manifestações dentro da família.
- Variantes de fatores de risco que condicionam um aumento relativo do risco de desenvolvimento de uma doença.
- Doenças de herança dominante, mitocondrial ou mendeliana.
- Variantes relacionadas com traços físicos não patológicos.
- Variantes de significado incerto ou sem evidências sobre seu efeito patogênico.
Por que os receptores também devem realizar um painel de portadores CGT para a seleção?
O objetivo do CGT não é realizar a seleção de pessoas não portadoras de mutações, pois mutações genéticas são comuns no ser humano, seria inviável um banco de gametas com doadores que não portem nenhuma mutação. O propósito de realizar o CGT é a possibilidade de comparar os painéis de portadores para identificar mutações em comum das partes que irão gerar um embrião. Estudos realizados pela Igenomix em banco de óvulos com base nos painéis portadores mais amplos e de melhor qualidade disponíveis no mercado revelam que em média, pessoas saudáveis são portadoras de cerca de 2 mutações. Por isso doadores jovens, assim como qualquer outra pessoa independente de sua idade, estão sujeitos a serem portadores de mutações e isso não afeta sua saúde. Uma mutação genética pode permanecer em uma família por muitas gerações sem que ninguém manifeste uma doença. O cuidado de descartar doadores que possam gerar um aumento de risco de doenças monogênicas é uma precaução básica que os bancos de óvulos e de sêmen oferecem através do teste de compatibilidade genética. Lembrando que o teste PGT-A, realizado para rastrear alterações cromossômicas nos embriões não analisa as doenças monogênicas.Qual é o risco de doenças autossômicas recessivas rastreadas no CGT?
Risco de doença genética de herança autossômica recessiva existe quando o Homem e a Mulher que darão origem ao embrião são portadores de uma mesma mutação genética: Na formação de um embrião, se o óvulo e o espermatozoide portarem uma mesma mutação recessiva, existe um risco de 25% de nascimento de um bebê afetado por uma doença genética sem cura.
Na formação de um embrião, se o óvulo e o espermatozoide portarem uma mesma mutação recessiva, existe um risco de 25% de nascimento de um bebê afetado por uma doença genética sem cura.
Estratégia de prevenção de riscos de doenças genéticas
Para evitar as doenças genéticas mais frequentes e doenças genéticas de mutações específicas que se têm conhecimento na família, os bancos de óvulos, assim como os bancos de sêmen realizam painéis genéticos de diferentes amplitudes para auxiliar na seleção de doadores com risco reduzido de doenças hereditárias. Além disso, no caso da seleção de doadoras de óvulos, o risco de mutações genéticas ligadas ao cromossomo sexual feminino (X) precisa ser considerado para prevenir o nascimento de um menino afetado pela Síndrome do X Frágil, uma doença com sintomas similares ao espectro autista. A gravidade desta alteração é muito maior para os meninos porque as meninas possuem dois cromossomos X, portanto existe uma compensação para o caso delas, o que reduz os sintomas, sendo a principal ameaça para as meninas uma possível falência prematura ovariana.
Painel genético CGT Bank
O CGT Bank é o painel de portadores (Carrier Screening) ideal para banco de óvulos porque estuda um total de 71 doenças. Incluindo as doenças autossômicas recessivas mais comuns, além genes ligados a doenças que afetam o cromossomo X. Algumas das condições analisadas são: RECESSIVOS- CFTR – Fibrose Cística
- HBA1/HBA2 – Alfa Talassemia
- HBB – Beta Talassemia
- GJB2 – Surdez Hereditária Autossômica recesiva
- SMN1 – Atrofia Muscular Espinhal
- FMR1 – Síndrome de X frágil
- G6PD – Anemia hemolítica por déficit de G6PD
Desconfie quando não há informação sobre mutações genéticas
É pouco comum que uma pessoa não possua mutações genéticas. Se um banco de óvulos decidisse aceitar apenas candidatos que não portem nenhuma alteração desse tipo, isso reduziria os bancos em 80% e certamente não estaria excluindo pessoas portadoras, mas apenas portadores das mutações conhecidas. A solução mais efetiva para prevenir o risco de doenças genéticas tem sido realizar teste CGT e posterior “matching”, conhecido como teste compatibilidade genética para identificar coincidências entre as mutações dos doadores em relação ao DNA à pessoa da família receptora que aportará o espermatozoide ou óvulo.Mesmo quando são realizados painéis de portadores e compatibilidade genética que minimizam o risco do futuro bebê manifestar uma doença genética, não é possível excluir 100% dos riscos já que podem existir doenças raras não contidas no painel, bem o como o risco da manifestação de uma mutação “de novo”, ou seja, que surge por primeira vez em uma família sem herança genética.Nenhum teste pode prevenir 100% das doenças genéticas
Cariótipo dos doadores é fundamental
Assim como o cariótipo é um exame básico para o casal em tratamento de fertilidade, no caso de doadores sua importância é a mesma, já que pessoas completamente assintomáticas podem ser portadoras de alterações cromossômicas que aumentam o risco de aborto, falhas de implantação e descendência afetada por síndromes genéticas. Alguns achados no cariótipo do doador serão fatores de exclusão dos candidatos a doação de gametas:- Translocações recíprocas
- Translocações robertsonianas
- Inversões pericêntricas e paracêntricas
- Doadoras de óvulos com alguma variante patogênica ligada ao cromossomo X, que no caso dos homens se descartam já na triagem clínica.
- Alterações cromossômicas numéricas
Premissas básicas para a aplicação de um teste de portadores no programa de doação de gametas
- É preciso que exista um consenso sobre os benefícios do ponto de vista da equipe clínica e dos pacientes.
- O objetivo é evitar um problema de saúde grave
- Deve existir assessoramento científico e aconselhamento genético anterior e posterior à análise genética.



