O que é o teste ERA®
- ERA® é o teste desenvolvido para avaliar a receptividade endometrial patenteado pela Igenomix em 2009 (PCT/ ES2009/000386).
- O ERA® é o primeiro teste de diagnóstico que determina o momento único e personalizado de transferência de embriões de cada mulher, sincronizando assim a transferência de embriões com a janela individualizada de implantação.
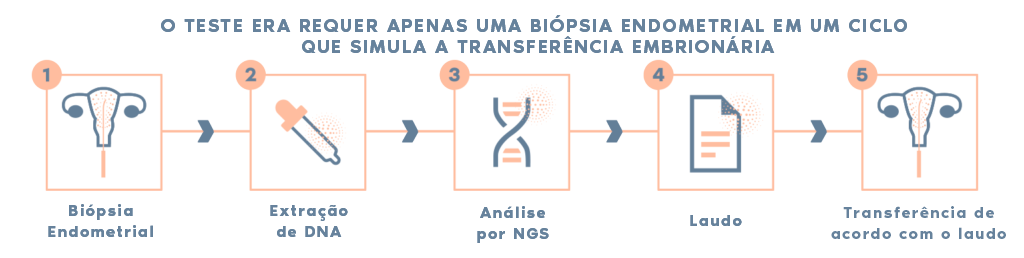
Como é o procedimento?
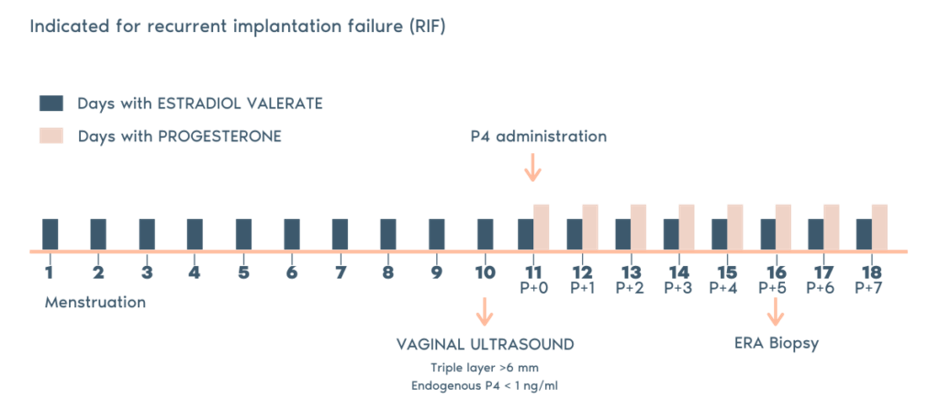
- O médico especialista realiza uma biópsia endometrial em um ciclo que simula o procedimento de preparo para a transferência embrionária.
- Após a extração do RNA da amostra recibida, a Igenomix realiza a análise da expressão dos genes ligados à receptividade endometrial.
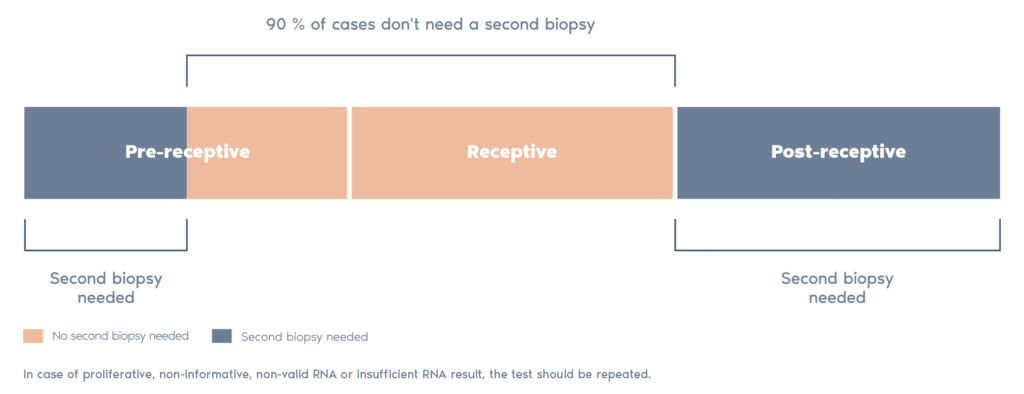
- O resultado da análise aponta se o endométrio está ou não receptivo para o tipo de protocolo utilizado ou será necessário uma adaptação, conforme recomendação do laudo.
- Em 90% dos casos não é preciso repetir a biópsia endometrial.
- Para realizar a transferência de acordo com a indicação do teste ERA é preciso manter a mesma via de administração da progesterona realizada na coleta da biópsia endometrial.